Trong thế giới hóa học hữu cơ phong phú, việc hiểu và viết công thức cấu tạo và gọi tên của C4H8O2 là một kỹ năng cơ bản nhưng vô cùng quan trọng. C4H8O2 là một công thức phân tử thú vị, đại diện cho một loạt các hợp chất hữu cơ khác nhau, chủ yếu thuộc nhóm axit cacboxylic và este, mỗi loại mang trong mình những đặc tính và ứng dụng riêng biệt. Bài viết này của lophoctichcuc.com sẽ đi sâu vào phân tích công thức C4H8O2, hướng dẫn bạn cách xác định và biểu diễn các đồng phân cấu tạo một cách chính xác, đồng thời trình bày các quy tắc gọi tên theo danh pháp IUPAC, giúp bạn nắm vững kiến thức nền tảng và áp dụng hiệu quả vào việc học tập và nghiên cứu hóa học.
Tổng Quan Về C4H8O2 và Các Đồng Phân Cơ Bản
Công thức phân tử C4H8O2 cho chúng ta biết rằng hợp chất này bao gồm 4 nguyên tử cacbon, 8 nguyên tử hiđro và 2 nguyên tử oxi. Để bắt đầu xác định các đồng phân cấu tạo, chúng ta cần tính toán độ bất bão hòa (k) của công thức này. Công thức tính độ bất bão hòa (k) cho hợp chất hữu cơ là: k = (2C + 2 + N - H - X) / 2, trong đó C, N, H, X lần lượt là số nguyên tử cacbon, nitơ, hiđro và halogen. Đối với C4H8O2, không có nitơ và halogen, nên công thức trở thành: k = (2 4 + 2 - 8) / 2 = (8 + 2 - 8) / 2 = 2 / 2 = 1.
Giá trị k = 1 cho biết rằng trong cấu trúc của các đồng phân C4H8O2 sẽ có một liên kết pi (π) hoặc một vòng no. Với sự hiện diện của hai nguyên tử oxi, các nhóm chức có thể chứa liên kết pi là nhóm cacboxyl (-COOH) hoặc nhóm este (-COO-). Cả hai nhóm chức này đều chứa một liên kết C=O, đóng góp đúng một độ bất bão hòa (k=1). Do đó, các đồng phân chính mà chúng ta sẽ tập trung vào là axit cacboxylic và este đơn chức, no, mạch hở. Bên cạnh đó, cũng có thể tồn tại các loại đồng phân khác như hydroxy-andehit, hydroxy-xeton, hoặc diol không no, nhưng trong chương trình hóa học phổ thông, axit cacboxylic và este là trọng tâm khi xét đến công thức CnH2nO2. Để hiểu rõ hơn về các loại công thức este, bạn có thể tham khảo bài viết về công thức este đơn chức trên trang web của chúng tôi.
Việc xác định các đồng phân cấu tạo của C4H8O2 đòi hỏi một phương pháp tiếp cận hệ thống, bắt đầu từ việc xem xét các loại nhóm chức có thể có, sau đó là cách sắp xếp mạch cacbon và vị trí của các nhóm chức đó. Quá trình này không chỉ giúp chúng ta nhận diện được từng hợp chất riêng lẻ mà còn củng cố kiến thức về danh pháp hóa học hữu cơ, cho phép chúng ta gọi tên chúng một cách chính xác.
Đồng Phân Axit Cacboxylic C4H8O2
Các axit cacboxylic là những hợp chất hữu cơ chứa nhóm cacboxyl (-COOH). Với công thức phân tử C4H8O2 và độ bất bão hòa k=1, nhóm cacboxyl chính là yếu tố tạo nên liên kết pi. Việc còn lại là sắp xếp 3 nguyên tử cacbon còn lại vào mạch chính.
Axit Butanoic (Axit n-butyric)
Đây là đồng phân axit cacboxylic mạch thẳng. Mạch cacbon gồm 4 nguyên tử cacbon liên kết với nhau thành một chuỗi không phân nhánh, trong đó nhóm cacboxyl được đặt ở một đầu mạch.
- Công thức cấu tạo: CH3-CH2-CH2-COOH
- Giải thích cấu tạo: Nguyên tử cacbon thứ nhất của chuỗi liên kết với nhóm cacboxyl. Ba nguyên tử cacbon còn lại tạo thành một mạch thẳng.
- Tên gọi IUPAC: Axit butanoic. Tên này được hình thành từ tên ankan tương ứng (butan) và hậu tố “-oic” kèm theo từ “axit”. Số “1” để chỉ vị trí nhóm cacboxyl thường được bỏ qua vì nó luôn ở đầu mạch và được đánh số 1.
- Tên gọi thông thường: Axit n-butyric. Từ “n-” chỉ mạch thẳng không phân nhánh. Axit butyric là một axit béo có trong bơ.
- Tính chất và ứng dụng: Axit butanoic là một chất lỏng không màu, có mùi khó chịu, thường thấy trong bơ ôi, phô mai parmesan và mồ hôi. Nó hòa tan tốt trong nước và là một axit yếu. Trong công nghiệp, axit butanoic được sử dụng để sản xuất este (ví dụ: metyl butanoat, etyl butanoat) dùng làm hương liệu thực phẩm và nước hoa.
Axit 2-Metylpropanoic (Axit Isobutyric)
Đây là đồng phân axit cacboxylic có mạch cacbon phân nhánh. Mạch chính chứa nhóm cacboxyl chỉ có 3 nguyên tử cacbon, và có một nhóm metyl (-CH3) làm nhánh.
- Công thức cấu tạo: (CH3)2CH-COOH hoặc viết rõ hơn là CH3-CH(CH3)-COOH
- Giải thích cấu tạo: Mạch chính có 3 cacbon (từ nhóm cacboxyl đến cacbon xa nhất). Nhóm metyl (-CH3) được gắn vào nguyên tử cacbon số 2 của mạch chính (khi đánh số từ cacbon của nhóm cacboxyl).
- Tên gọi IUPAC: Axit 2-metylpropanoic. “Propanoic” là tên của axit cacboxylic có 3 cacbon, và “2-metyl” chỉ vị trí nhóm metyl trên cacbon số 2.
- Tên gọi thông thường: Axit isobutyric. Từ “iso-” chỉ cấu trúc phân nhánh đặc trưng với một nhóm CH3 ở cacbon thứ hai từ cuối mạch.
- Tính chất và ứng dụng: Axit 2-metylpropanoic cũng là một chất lỏng không màu với mùi tương tự axit butanoic. Nó là một đồng phân cấu tạo của axit butanoic và có tính chất hóa học tương tự. Nó được sử dụng trong sản xuất este cho nước hoa và hương liệu, cũng như trong tổng hợp các hợp chất hữu cơ khác.
Đồng Phân Este C4H8O2
Este là những hợp chất hữu cơ được tạo thành từ phản ứng giữa axit cacboxylic và ancol, có nhóm chức este (-COO-). Với công thức C4H8O2, các đồng phân este cũng là este đơn chức, no, mạch hở. Để viết công thức este, chúng ta cần phân chia 4 nguyên tử cacbon thành hai phần: một phần thuộc gốc axit (R-COO-) và một phần thuộc gốc ancol (-R’).
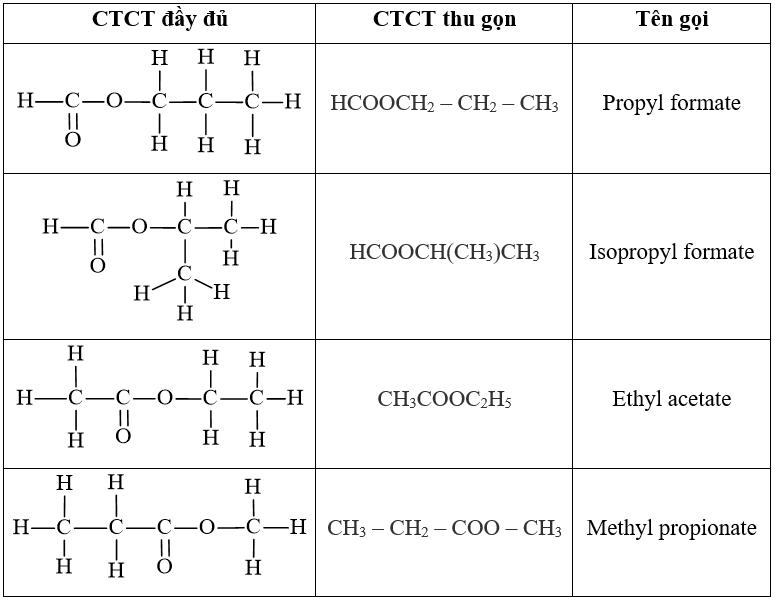
1. Metyl Propanoat
Đây là este được tạo thành từ axit propanoic và metanol.
- Công thức cấu tạo: CH3-CH2-COO-CH3
- Giải thích cấu tạo: Gốc axit là propanoat (CH3-CH2-COO-), có 3 nguyên tử cacbon. Gốc ancol là metyl (-CH3), có 1 nguyên tử cacbon.
- Tên gọi IUPAC: Metyl propanoat. “Metyl” là tên gốc hiđrocacbon của ancol (metanol), “propanoat” là tên của anion gốc axit propanoic.
- Tính chất và ứng dụng: Metyl propanoat là chất lỏng không màu, có mùi trái cây nhẹ, thường được sử dụng làm dung môi hoặc trong công nghiệp hương liệu. Để hiểu rõ hơn về cách các este như thế này có thể được thủy phân, bạn có thể tham khảo bài viết về thủy phân este x mạch hở có công thức c4h6o2.
2. Etyl Axetat
Đây là este được tạo thành từ axit axetic và etanol.
- Công thức cấu tạo: CH3-COO-CH2-CH3
- Giải thích cấu tạo: Gốc axit là axetat (CH3-COO-), có 2 nguyên tử cacbon. Gốc ancol là etyl (-CH2-CH3), có 2 nguyên tử cacbon.
- Tên gọi IUPAC: Etyl axetat. “Etyl” là tên gốc hiđrocacbon của ancol (etanol), “axetat” là tên của anion gốc axit axetic.
- Tính chất và ứng dụng: Etyl axetat là một trong những este phổ biến nhất, là chất lỏng không màu, có mùi thơm dễ chịu của trái cây (đặc biệt là lê). Nó được sử dụng rộng rãi làm dung môi trong sơn móng tay, keo dán, mực in, và trong công nghiệp thực phẩm, dược phẩm.
3. Propyl Fomat
Đây là este được tạo thành từ axit fomic (axit metanoic) và propanol-1 (n-propanol).
- Công thức cấu tạo: H-COO-CH2-CH2-CH3
- Giải thích cấu tạo: Gốc axit là fomat (H-COO-), chỉ có 1 nguyên tử cacbon. Gốc ancol là propyl (-CH2-CH2-CH3), có 3 nguyên tử cacbon mạch thẳng.
- Tên gọi IUPAC: Propyl fomat. “Propyl” là tên gốc hiđrocacbon của ancol (propanol), “fomat” là tên của anion gốc axit fomic (hoặc metanoat).
- Tính chất và ứng dụng: Propyl fomat là chất lỏng không màu, có mùi trái cây, thường được sử dụng làm hương liệu thực phẩm và trong sản xuất các hợp chất hữu cơ khác.
4. Isopropyl Fomat
Đây là este được tạo thành từ axit fomic (axit metanoic) và isopropanol (propanol-2).
- Công thức cấu tạo: H-COO-CH(CH3)2
- Giải thích cấu tạo: Gốc axit là fomat (H-COO-), chỉ có 1 nguyên tử cacbon. Gốc ancol là isopropyl (-CH(CH3)2), có 3 nguyên tử cacbon phân nhánh.
- Tên gọi IUPAC: Isopropyl fomat. “Isopropyl” là tên gốc hiđrocacbon của ancol (isopropanol), “fomat” là tên của anion gốc axit fomic.
- Tính chất và ứng dụng: Isopropyl fomat là một đồng phân cấu tạo của propyl fomat, cũng là chất lỏng có mùi trái cây, được sử dụng tương tự trong ngành công nghiệp hương liệu.
Nguyên Tắc Gọi Tên Hợp Chất Hữu Cơ (IUPAC) và Ứng Dụng Cho C4H8O2
Hệ thống danh pháp IUPAC (International Union of Pure and Applied Chemistry) cung cấp một bộ quy tắc thống nhất để gọi tên các hợp chất hóa học, đảm bảo mỗi công thức cấu tạo chỉ có một tên duy nhất và ngược lại. Điều này đặc biệt quan trọng khi chúng ta cần viết công thức cấu tạo và gọi tên của C4H8O2 với nhiều đồng phân.
Đối với Axit Cacboxylic
- Chọn mạch chính: Là mạch cacbon dài nhất chứa nhóm cacboxyl (-COOH).
- Đánh số mạch chính: Bắt đầu từ nguyên tử cacbon của nhóm cacboxyl (luôn là C1).
- Gọi tên:
- Tên gọi bắt đầu bằng từ “Axit”.
- Tiếp theo là tên ankan tương ứng với số nguyên tử cacbon của mạch chính.
- Kết thúc bằng hậu tố “-oic”.
- Nếu có nhóm thế, gọi tên và vị trí nhóm thế trước tên ankan.
- Ví dụ với C4H8O2:
- Axit butanoic: Mạch chính 4 cacbon, không có nhóm thế. -> Axit + butan + oic = Axit butanoic.
- Axit 2-metylpropanoic: Mạch chính 3 cacbon (propan), có nhóm metyl (-CH3) ở vị trí C2. -> Axit + 2-metyl + propan + oic = Axit 2-metylpropanoic.
Đối với Este
- Xác định gốc ancol (R’): Phần hiđrocacbon liên kết với nguyên tử oxi đơn của nhóm este (-O-R’).
- Xác định gốc axit (R-COO-): Phần còn lại của este, bao gồm nguyên tử cacbon của nhóm cacboxyl.
- Gọi tên:
- Tên gọi bắt đầu bằng tên gốc hiđrocacbon của ancol (ví dụ: metyl, etyl, propyl, isopropyl).
- Tiếp theo là tên anion gốc axit, được hình thành bằng cách thay thế hậu tố “-oic” của axit cacboxylic bằng “-oat” (hoặc “-ic” bằng “-at” đối với tên thông thường).
- Ví dụ với C4H8O2:
- Metyl propanoat: Gốc ancol là metyl. Gốc axit từ axit propanoic -> propanoat. -> Metyl propanoat.
- Etyl axetat: Gốc ancol là etyl. Gốc axit từ axit axetic -> axetat. -> Etyl axetat.
- Propyl fomat: Gốc ancol là propyl. Gốc axit từ axit fomic -> fomat (hoặc metanoat). -> Propyl fomat.
- Isopropyl fomat: Gốc ancol là isopropyl. Gốc axit từ axit fomic -> fomat. -> Isopropyl fomat.
Việc nắm vững các quy tắc này là chìa khóa để giải quyết hiệu quả các bài tập về danh pháp và cấu tạo hợp chất hữu cơ. Nếu bạn quan tâm đến việc xác định công thức cấu tạo của các hợp chất khác, một ví dụ khác là tìm hiểu c6h12o2 có bao nhiêu công thức cấu tạo, điều này sẽ giúp bạn mở rộng tư duy về đồng phân.
Các Đồng Phân Khác Của C4H8O2 (Nâng Cao)
Mặc dù axit cacboxylic và este là những đồng phân phổ biến nhất của C4H8O2 trong chương trình hóa học phổ thông, công thức này vẫn có thể đại diện cho các nhóm chức khác, đòi hỏi một sự phân tích sâu hơn về cấu trúc hóa học. Sự tồn tại của hai nguyên tử oxi và độ bất bão hòa k=1 mở ra nhiều khả năng khác, mặc dù chúng thường ít được đề cập hơn do độ phức tạp hoặc ít tính ứng dụng trong các bài toán cơ bản.
Một số loại đồng phân nâng cao có thể kể đến bao gồm:
1. Diol Không No
Diol là hợp chất chứa hai nhóm -OH. Với k=1, đồng phân diol có thể chứa một liên kết đôi C=C. Ví dụ, buten-diol có thể là một trong những đồng phân đó.
- Ví dụ: But-3-en-1,2-diol (CH2=CH-CH(OH)-CH2OH). Đây là một hợp chất có một liên kết đôi C=C (k=1) và hai nhóm hydroxyl. Việc gọi tên các hợp chất này tuân theo quy tắc IUPAC cho anken và ancol, với việc chỉ rõ vị trí của liên kết đôi và các nhóm hydroxyl.
2. Hydroxy Andehit và Hydroxy Xeton
Đây là các hợp chất có cả nhóm hydroxyl (-OH) và nhóm cacbonyl (C=O) của andehit (-CHO) hoặc xeton (>C=O). Nhóm cacbonyl đã đóng góp một độ bất bão hòa (k=1).
-
Hydroxy Andehit:
- 4-hydroxybutanal: HO-CH2-CH2-CH2-CHO. Nhóm -CHO ở cuối mạch, nhóm -OH ở vị trí cacbon thứ 4.
- 3-hydroxybutanal: CH3-CH(OH)-CH2-CHO.
- 2-hydroxybutanal: CH3-CH2-CH(OH)-CHO. Việc gọi tên được thực hiện bằng cách xác định mạch chính chứa nhóm andehit, đánh số từ nhóm andehit và gọi tên nhóm -OH như một nhóm thế “hydroxy”.
-
Hydroxy Xeton:
- 1-hydroxybutan-2-on: HO-CH2-CO-CH2-CH3. Nhóm xeton ở C2, nhóm -OH ở C1.
- 3-hydroxybutan-2-on: CH3-CH(OH)-CO-CH3. Quy tắc gọi tên tương tự, chọn mạch chính chứa nhóm xeton, đánh số sao cho nhóm xeton có số nhỏ nhất, và gọi tên nhóm -OH.
3. Ete Vòng Có Nhóm Hydroxyl
Các hợp chất vòng cũng đóng góp một độ bất bão hòa (k=1). Khi kết hợp với hai nguyên tử oxi, có thể tạo thành các ete vòng chứa nhóm hydroxyl.
- Ví dụ: Tetrahydrofuran-2-metanol (hay 2-(hydroxymetyl)oxolan) là một ete vòng 5 cạnh có một nhóm metanol gắn vào vòng. Tuy nhiên, công thức của nó là C5H10O2, không phải C4H8O2. Để có C4H8O2, chúng ta có thể xem xét các ete vòng 3 hoặc 4 cạnh với nhóm hydroxyl.
- 2-hydroxymetyl-oxiran: CH2(OH)-CH-CH2 (vòng 3 cạnh, CH2-O-CH).
- 3-hydroxytetrahydrofuran: Một vòng 5 cạnh (4C + 1O) với một nhóm OH. Các đồng phân này thường phức tạp hơn và đòi hỏi kiến thức sâu hơn về hóa học vòng.
Mặc dù việc xác định và gọi tên các đồng phân nâng cao này có thể không phải là trọng tâm chính khi học viết công thức cấu tạo và gọi tên của C4H8O2 ở cấp độ cơ bản, nhưng việc biết về sự tồn tại của chúng thể hiện sự hiểu biết toàn diện về cấu trúc và danh pháp hóa học hữu cơ. Nó cũng giúp người học phát triển tư duy logic và khả năng phân tích cấu trúc phức tạp, làm nền tảng cho việc tìm hiểu các hợp chất hữu cơ phức tạp hơn trong tương lai.
Phương Pháp Tiếp Cận Hệ Thống Để Viết Công Thức Cấu Tạo Và Gọi Tên
Để viết công thức cấu tạo và gọi tên của C4H8O2 một cách đầy đủ và chính xác, việc áp dụng một phương pháp tiếp cận có hệ thống là cực kỳ quan trọng. Phương pháp này giúp tránh bỏ sót đồng phân và đảm bảo tính logic trong quá trình xác định.
Bước 1: Tính Độ Bất Bão Hòa (k)
Như đã thực hiện ở phần đầu, tính k = (2C + 2 - H)/2 cho các hợp chất chỉ chứa C, H, O. Với C4H8O2, k = 1. Giá trị này là chìa khóa để xác định loại liên kết hoặc vòng có thể có.
Bước 2: Liệt Kê Các Nhóm Chức Có Thể Có
Dựa trên công thức phân tử và độ bất bão hòa, xác định các nhóm chức có thể tồn tại.
- Với C4H8O2 và k=1, có 2 nguyên tử oxi:
- Nhóm cacboxyl (-COOH): Chiếm k=1.
- Nhóm este (-COO-): Chiếm k=1.
- Nhóm cacbonyl (C=O) của anđehit/xeton kết hợp với nhóm hiđroxyl (-OH): Chiếm k=1.
- Liên kết đôi C=C kết hợp với hai nhóm hiđroxyl (-OH): Chiếm k=1.
- Vòng no kết hợp với hai nhóm hiđroxyl (-OH) hoặc một nhóm cacbonyl và một nhóm hiđroxyl: Chiếm k=1.
Bước 3: Xác Định Các Loại Đồng Phân Dựa Trên Nhóm Chức
1. Đồng Phân Axit Cacboxylic:
- Bắt đầu với nhóm -COOH.
- Còn lại 3 cacbon (C3H7) để tạo gốc ankyl.
- Vẽ các mạch cacbon có thể có với 3 cacbon:
- Mạch thẳng: -CH2-CH2-CH3 -> Axit butanoic.
- Mạch nhánh: -CH(CH3)2 -> Axit 2-metylpropanoic.
2. Đồng Phân Este:
- Este có dạng R-COO-R’. Tổng số C = 4.
- Liệt kê các khả năng phân chia cacbon giữa R và R’:
- Gốc axit 1C (HCOO-): Gốc fomat.
- Gốc ancol 3C: -CH2-CH2-CH3 (propyl) -> Propyl fomat.
- Gốc ancol 3C: -CH(CH3)2 (isopropyl) -> Isopropyl fomat.
- Gốc axit 2C (CH3COO-): Gốc axetat.
- Gốc ancol 2C: -CH2-CH3 (etyl) -> Etyl axetat.
- Gốc axit 3C (CH3CH2COO-): Gốc propanoat.
- Gốc ancol 1C: -CH3 (metyl) -> Metyl propanoat.
- (Gốc axit 4C là axit butanoic, không còn C cho gốc ancol)
- Gốc axit 1C (HCOO-): Gốc fomat.
3. Đồng Phân Hydroxy Anđehit/Xeton (nếu yêu cầu nâng cao):
- Anđehit: Đặt nhóm -CHO. Còn lại 3 cacbon và 1 nhóm -OH.
- HO-CH2-CH2-CH2-CHO (4-hydroxybutanal)
- CH3-CH(OH)-CH2-CHO (3-hydroxybutanal)
- CH3-CH2-CH(OH)-CHO (2-hydroxybutanal)
- Xeton: Đặt nhóm >C=O. Còn lại 3 cacbon và 1 nhóm -OH.
- HO-CH2-CO-CH2-CH3 (1-hydroxybutan-2-on)
- CH3-CH(OH)-CO-CH3 (3-hydroxybutan-2-on)
Bước 4: Viết Công Thức Cấu Tạo Và Gọi Tên
- Sau khi xác định được các loại mạch cacbon và vị trí nhóm chức, vẽ rõ ràng từng công thức cấu tạo.
- Áp dụng các quy tắc IUPAC đã trình bày để gọi tên từng đồng phân một cách chính xác. Đảm bảo tên gọi phản ánh đúng cấu trúc và không gây nhầm lẫn. Cần lưu ý các nguyên tắc này khi bạn cũng muốn viết công thức cấu tạo của c4h6 và gọi tên hoặc các hợp chất khác.
- Kiểm tra lại xem có trùng lặp đồng phân hay bỏ sót nào không.
Phương pháp này giúp đảm bảo sự toàn diện và chính xác, đặc biệt khi xử lý các công thức phân tử có nhiều đồng phân. Nó cũng là một kỹ năng tư duy quan trọng trong hóa học hữu cơ, giúp người học phát triển khả năng hình dung và phân tích cấu trúc phân tử.
Tầm Quan Trọng Của Việc Hiểu Các Đồng Phân C4H8O2 Trong Hóa Học
Việc nắm vững cách viết công thức cấu tạo và gọi tên của C4H8O2 không chỉ là một bài tập lý thuyết mà còn mang ý nghĩa thực tiễn sâu sắc trong nhiều khía cạnh của hóa học và đời sống. Các hợp chất với công thức C4H8O2, đặc biệt là axit cacboxylic và este, đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau.
Trong Nghiên Cứu và Giáo Dục Hóa Học
- Nền tảng kiến thức: Việc học về các đồng phân của C4H8O2 là một phần thiết yếu trong chương trình hóa học hữu cơ. Nó giúp sinh viên và học sinh xây dựng nền tảng vững chắc về khái niệm đồng phân, nhóm chức, và danh pháp IUPAC. Đây là những kỹ năng cơ bản để tiếp cận với các hợp chất hữu cơ phức tạp hơn.
- Phát triển tư duy phân tích: Quá trình xác định các đồng phân đòi hỏi tư duy logic, khả năng hình dung không gian của phân tử và áp dụng các quy tắc một cách có hệ thống. Điều này rèn luyện kỹ năng giải quyết vấn đề và tư duy phản biện.
- Hiểu biết sâu hơn về tính chất hóa học: Mỗi đồng phân, mặc dù có cùng công thức phân tử, lại có cấu trúc và do đó có tính chất hóa học và vật lý khác nhau. Ví dụ, axit butanoic là một axit, phản ứng với bazơ và có mùi hôi, trong khi etyl axetat là một este, có mùi thơm trái cây và có thể tham gia phản ứng thủy phân. Hiểu được sự khác biệt này là chìa khóa để dự đoán phản ứng và ứng dụng của chúng.
Trong Công Nghiệp và Đời Sống
- Ngành công nghiệp thực phẩm và hương liệu: Nhiều este của C4H8O2, như etyl axetat, metyl propanoat, propyl fomat, isopropyl fomat, được sử dụng rộng rãi làm hương liệu để tạo mùi thơm trái cây cho thực phẩm, đồ uống và kẹo. Khả năng tạo ra các mùi hương khác nhau từ cùng một công thức phân tử là một minh chứng rõ ràng cho vai trò của đồng phân hóa học.
- Ngành dung môi: Etyl axetat là một dung môi công nghiệp phổ biến, được sử dụng trong sơn móng tay, keo dán, mực in, và trong quá trình sản xuất dược phẩm. Tính chất hòa tan tốt và bay hơi nhanh của nó làm cho nó trở thành lựa chọn ưu tiên trong nhiều ứng dụng.
- Ngành dược phẩm và hóa chất: Các axit cacboxylic như axit butanoic và axit 2-metylpropanoic có thể được sử dụng làm nguyên liệu thô hoặc chất trung gian trong tổng hợp các loại thuốc, polyme và các hóa chất hữu cơ khác. Sự hiểu biết về cấu trúc của chúng là cần thiết để thiết kế và tổng hợp các hợp chất mới.
Tóm lại, việc nghiên cứu các đồng phân của C4H8O2 không chỉ là một phần của chương trình học mà còn là cánh cửa mở ra sự hiểu biết về thế giới hóa học hữu cơ đầy màu sắc và ứng dụng rộng rãi. Nó giúp chúng ta không chỉ giải quyết các bài toán trên giấy mà còn hiểu được tại sao các chất khác nhau lại có những đặc tính và vai trò riêng biệt trong cuộc sống hàng ngày và trong các ngành công nghiệp. Việc học tập và nghiên cứu một cách kỹ lưỡng các đồng phân của C4H8O2, cùng với các hợp chất hữu cơ khác, sẽ trang bị cho người học những kiến thức và kỹ năng cần thiết để thành công trong lĩnh vực khoa học này.
Kết Luận
Qua bài viết này, chúng ta đã cùng nhau khám phá sâu rộng về cách viết công thức cấu tạo và gọi tên của C4H8O2, một công thức phân tử thú vị đại diện cho nhiều đồng phân quan trọng trong hóa học hữu cơ. Bằng việc áp dụng phương pháp tiếp cận hệ thống, từ việc tính toán độ bất bão hòa đến việc phân tích các nhóm chức và sắp xếp mạch cacbon, chúng ta đã xác định được hai đồng phân axit cacboxylic (axit butanoic và axit 2-metylpropanoic) và bốn đồng phân este (metyl propanoat, etyl axetat, propyl fomat, isopropyl fomat). Việc nắm vững các nguyên tắc danh pháp IUPAC cho phép chúng ta gọi tên từng đồng phân một cách chính xác, phản ánh đúng cấu trúc hóa học độc đáo của chúng. Sự khác biệt về cấu trúc này không chỉ là một khái niệm lý thuyết mà còn ảnh hưởng trực tiếp đến tính chất vật lý, hóa học và ứng dụng thực tiễn của từng hợp chất, từ hương liệu thực phẩm đến dung môi công nghiệp. Hy vọng rằng, những thông tin chi tiết này sẽ là nguồn tài liệu hữu ích, giúp bạn củng cố kiến thức và tự tin hơn trong việc giải quyết các bài toán liên quan đến công thức C4H8O2 và danh pháp hợp chất hữu cơ.


